一种病很要命,正常人进行运动或情绪过于激动只会引起心跳加快,而对于这类患者则可能导致昏厥,甚至心脏骤停及猝死,而且随着增龄,风险还会增进,这种病就是儿茶酚胺敏感室性心动过速(CPVT)。
如何寻找治疗这种遗传性致死性心律失常的更优方案,与死神竞速,“与心竞速”?
近期,Circulation发布了一项波士顿儿童医院、哈佛大学和湖北大学合作的里程碑式研究,该研究组利用人诱导性多能干细胞分化得到心肌细胞构建体外组织工程模型去破解CPVT的致病机理,首次实现了人源心肌微器官芯片对心律失常的体外建模,并找到了引起CPVT表型的功能性磷酸化位点,为心律失常相关药物的研发提供了直接的实验证据。
波士顿儿童医院心内科主任WilliamT.Pu教授和哈佛大学工程与科学学院器官芯片领军教授KevinKit Parker领衔,湖北大学张冬卉教授为共同第一作者。
构建心律失常组织
在心肌细胞中,RYR2就像一个可以控制钙离子进出的门,RYR2通道的突变会导致钙离子的非正常泄露,从而造成CPVT表型。
这项研究利用体外重编程技术,将CPVT患者的成纤维细胞变成具有全能性的诱导性多能干细胞,并进一步进行体外心肌分化,获得具有RYR2突变的心肌细胞。
“将细胞接种在图案化的材料表面,体外模拟心肌的同向排布方式,”张冬卉教授解释道,“得到心肌微组织可以实际地模拟患者心肌组织的电传导特性,这就是心肌微器官相比传统单细胞功能测试的优势。”
培养皿中的“跑步机”模型
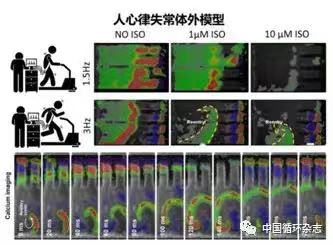
利用光遗传学系统代替电刺激,通过提高刺激心肌微组织的频率来模拟患者在跑步机上进行的测试。同时为了在体外模拟运动,研究者添加了异丙肾上腺素(类似于肾上腺素)来使组织更快跳动。
“当我们提高心肌的波动频率,CPVT组织会持续出现反复性心律失常,而正常组织则可以很好地响应高频率刺激,”Pu说。
进一步的研究发现在健康的心脏组织中,有一种CaMKII的酶可修饰RYR2,从而让RYR2开门使心肌细胞释放出更多的钙。在CPVT细胞中,这种修饰与突变的RYR2结合,导致门异常泄露,从而引起心律失常。
“大自然设计了CaMKII作为战斗或逃跑反应的一部分,”Pu解释道。
“当一个人兴奋的时候,会释放出更多的钙,这样心脏就可以更快地跳动。但是当RYR2发生突变时,通道就会渗漏,因此细胞会释放过多的钙,导致心律失常。”当研究人员阻止CaMKII修饰时,消除了组织模型中的心律失常。
当用肽AIP(一种有效的和选择性的CaMKII抑制剂)阻断CaMKII本身时,具有相同效果。
基因疗法治疗CPVT
利用基因编辑技术封闭CPVT患者细胞系中RYR2上可被CaMKII修饰的磷酸化位点,可以从根本上消除CPVT的疾病表型,研究者已在小鼠模型上成功验证这种基因疗法的有效性。
心血管病专家Eric Topol发推称“这项工作从患者来源诱导性多能干细胞到心肌分化、到心肌微器官芯片再到疾病模型,最终走向真正的基因修正治愈。”
张冬卉教授称“从临床到实验室,再回到临床一直是科研工作者最高的理想和追求,这个工作是个很好的开始,我们还将继续前进。”

张冬卉教授2010年博士毕业于北京大学,并于2011年-2017年先后在杜克大学、哈佛医学院开展博士后研究工作,2017年7月正式入职澳门尼威斯人网站8311任教授、博士生导师,并担任学院教工党支部第二支部书记。获湖北大学第一届“我心中的好导师”十佳奖。

自加入湖北大学近两年以来,她始终秉持育人为本的教育理念,指导在读研究生10人、本科生21人(其中,1名毕业生论文获评2018届校级优秀本科毕业论文、1名学生入选湖北大学2018年度国家级大学生创新创业训练计划项目),主讲遗传学、参讲生物工程技术前沿讲座、现代生物学导论等课程、总计40个学时;不仅如此,她还开办知识讲座、主讲学业指导,为大一新生打开生物学新世界的大门、为考研学子指点迷津。
除了为教书育人鞠躬尽瘁,她在科研道路上更是勇往无前,近2年共发表SCI论文6篇、中文核心期刊论文2篇、参编教材1部、主持国家自然科学基金2项并以项目骨干身份参与国家重点研发计划1项,受邀参加国内多场高水平会议,并应邀前往华中科技大学、武汉大学人民医院、武汉科技大学、武汉纺织大学等高校做学术报告。她面对学术研究的拼搏与严谨始终作为一盏长明灯为后来者照亮前进的路。
来源:http://www.hubu.edu.cn/info/1075/31532.htm?tdsourcetag=s_pcqq_aiomsg




