近日,澳门尼威斯人网站8311、省部共建生物催化与酶工程国家重点实验室郭瑞庭教授团队与武汉大学药学院周海兵教授团队合作,在国际重要学术期刊Acta Pharmaceutica Sinica B(APSB)发表了题为“Discovery of novel covalent selective estrogen receptor degraders against endocrine-resistant breast cancer”的研究论文。该研究发现了一款新型共价雌激素受体降解剂,并通过晶体学和质谱研究验证了其作用机制,为内分泌耐药型乳腺癌药物的研发提供了候选化合物。郭瑞庭教授、董春娥教授和周海兵教授为本文共同通讯作者,武汉大学博士生王禹博、邓湘萍以及湖北大学闵鉴副教授为本文共同第一作者。
乳腺癌严重威胁着女性健康,给社会和经济造成巨大负担。大约70%的患者是雌激素受体(Estrogen Receptor, ER)阳性乳腺癌,临床上均需接受内分泌治疗。然而,绝大部分患者在内分泌治疗过程中出现耐药,病情容易进展为晚期乳腺癌。选择性雌激素受体降解剂(selective estrogen receptor degraders, SERDs)能够诱导ER蛋白降解,具有克服耐药性的潜力。目前,临床上唯一批准的SERD为氟维司群,但其不良的药代性质极大限制了临床应用。内分泌和靶向治疗ER+乳腺癌药物的临床需求巨大,与之对应的是5年生存率约为30%。因此,设计开发新型SERD,具有重要的科学意义和临床价值。
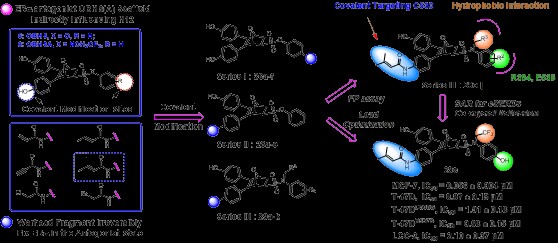
药物设计与药物发现
本研究以5,6-二芳基-7-氧代双环[2.2.1]庚-5-烯(5,6-diaryl-7-oxabicyclo [2.2.1]hept-5-ene N-aryl sulfonamide, OBHS)结构为核心骨架为先导化合物,通过理性设计及多轮分子优化,获得可以与ER耐药突变位点Y537S结合口袋中第530位半胱氨酸形成共价键的化合物29c,并通过晶体结构进行了验证。抑制剂分子在耐药乳腺癌肿瘤细胞模型和动物模型中展现出了良好的抑制活性和抗癌活性,并显著诱导ER蛋白降解。研究结果验证了共价靶向ER降解的开发策略,为临床抗内分泌耐药型乳腺癌药物提供了新选择。
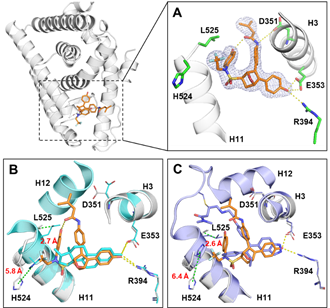
29c与雌激素受体晶体结构解析
郭瑞庭教授团队长期从事药物靶点、高分子生物降解酶,以及新型萜类合成酶的结构解析与机理探讨的研究,在Nature Catalysis、Immunity、JACS、Angewandte Chemie、Nature Communications、ACS Catalysis等国际知名期刊上发表多篇高水平文章,研究工作得到国家重大专项、国家自然科学基金和湖北省创新群体等基金的支持。
论文连接:https://www.sciencedirect.com/science/article/pii/S221138352300151X




